HTA ist die Abkürzung für Health Technology Assessment und bezeichnet die systematische Bewertung von gesundheitsrelevanten Verfahren, Prozessen, Technologien und Hilfsmitteln.
Inhaltsverzeichnis
HTA – Grundlegende Informationen
Historie
Im Jahr 1965 wurde erstmals der Begriff „Technology Assessment“ im US-Kongress erwähnt und umfasste damals Transportwesen und Verkehr sowie Ernährung und Raumfahrt. Zwischen 1970 und 1980 wurde auch dem Gesundheitswesen mehr Beachtung geschenkt, sodass erste Konzepte zur Technologiebewertung im Gesundheitswesen entstanden. Erste Gremien gründeten sich 1972 (z. B. das Office of Technology Assessment (OTA)) und Mitte der 1980er Jahre begann auch Europa, den Fokus auf die Technologiebewertung im Gesundheitswesen zu legen. 1985 wurde das wichtigste Forum für HTA-Fragen gegründet: die International Society of Technology Assessment in Health Care (ISTAHC), die seit 2003 nunmehr Health Technology Assessment International (HTAI) heißt.
In Deutschland wurde im Jahr 1994 das Büro für Technologieabschätzung beim Deutschen Bundestag gegründet und im darauffolgenden Jahr ein HTA-Programm eingerichtet. Im Jahr 2000 übernahm das Deutsche Institut für Medizinische Dokumentation und Information (DIMDI) das HTA-Programm. Im Zuge dessen wurde die Deutsche Agentur für Health Technology Assessment des DIMDI (DAHTA@DIMDI) gegründet. Trotz Übernahme wesentlicher Funktionen des DIMDI durch das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) im Jahr 2020 fungiert diese Datenbank weiterhin unter der genannten Bezeichnung. Seit 2004 erstellt auch das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) entsprechende Gutachten/-Berichte.
Vorgehensweise zur HTA-Berichterstellung
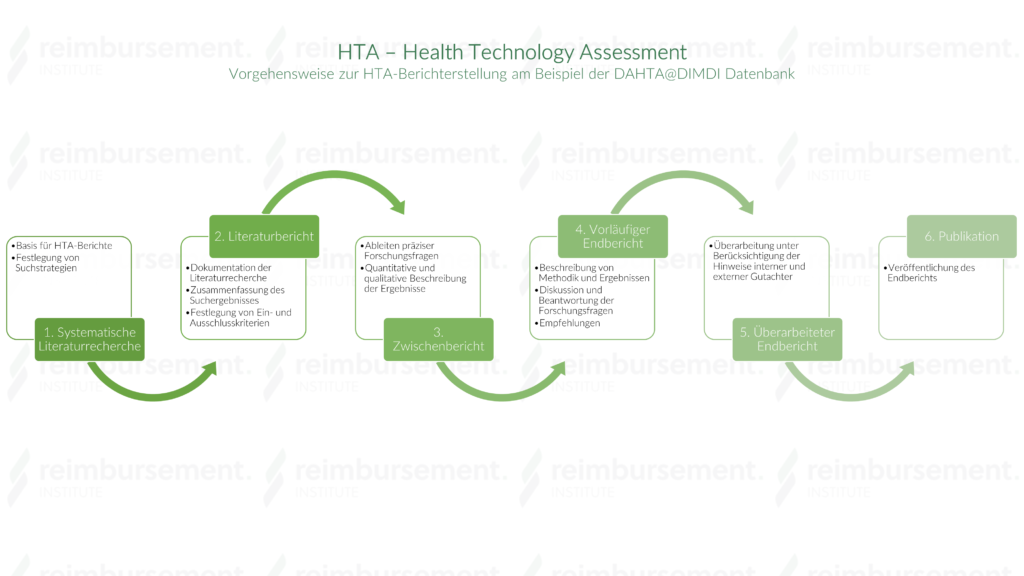
Vorgehensweise des DIMDI
- Systematische Literaturrecherche
- Basis für HTA-Berichte
- Festlegung von Suchstrategie mit relevanten Schlagwörtern
- Recherche führt DAHTA durch
- Literaturbericht
- Dokumentation der Literaturrecherche
- Zusammenfassung des Suchergebnisses: gesundheitspolitischer Hintergrund und wissenschaftliche Fragen zum Thema
- Festlegung von Ein- und Ausschlusskriterien
- Zwischenbericht
- Gesundheitspolitischer und wissenschaftlicher Hintergrund
- Ableiten präziser Forschungsfragen
- Quantitative und qualitative Beschreibung der Ergebnisse
- vorläufiger Endbericht
- Beschreibung von Methodik und Ergebnissen
- Diskussion und Beantwortung der Forschungsfragen
- Empfehlungen
- überarbeiteter Endbericht
- Überarbeitung unter Berücksichtigung der Hinweise interner und externer Gutachter
- Publikation
- Veröffentlichung des Endberichts in der DAHTA-Datenbank und im gms e-journal
Health Technology Assessment kann als eine Art Entscheidungsunterstützung oder Hilfestellung für Leistungserbringer herangezogen werden, wenn Vorgehensweisen bei der Behandlung von Patienten zur Diskussion stehen. Da entsprechende Berichte auch oft unter ökonomischen Aspekten erstellt werden, kann dies die Streichung von Technologien aus dem GKV-Leistungskatalog (GKV – Gesetzliche Krankenversicherung) bewirken. Die Berichte führen zu einer optimierten Planbarkeit und Kostenabschätzung, müssen jedoch stets individuell auf den einzelnen Fall angewendet werden.